Futurs traitements de l'hépatite C chronique
L'hépatite C chronique est une « épidémie » mondiale avec environ 200 millions de personnes actuellement infectées par le virus de l'hépatite C (VHC). Le génotype du VHC prédominant est le génotype 1 (GT1). Bien que la taille de la population ayant une infection chronique par le VHC ait été stable depuis 2000, c'est une cohorte vieillissante et la proportion de cette cohorte avec une cirrhose va doubler au cours de la prochaine décennie. Moins de 10% de la population infectée a été traitée et moins de la moitié de ces patients ont été guéris.
Le standard de soins actuel pour le traitement de l’hépatite C chronique est une association d'interféron pégylé et de ribavirine (PEG-INF/RBV) pendant 24 ou 48 semaines. Il n'est malheureusement associé qu'à une efficacité (45% pour le VHC GT1, 75% pour GT2 et 65% pour GT3) et une tolérance faibles. Beaucoup de patients, y compris ceux ayant une cirrhose décompensée ou des maladies psychiatriques sévères, sont soit inaptes pour, ou déclinent, le traitement actuel en raison des effets secondaires importants qui lui sont associés. L'ajout d'un inhibiteur de la protéase à PEG-INF/RBV est associé avec une augmentation de l'efficacité et une réduction de la durée de la thérapie chez les patients atteints du VHC GT1 et est en train de devenir le nouveau standard de soins pour le VHC GT1. Cependant, la trithérapie n’est pas adaptée aux patients ayant une infection par le VHC non-GT1, ou une contre-indication à l'interféron.
Les prédicteurs de non-réponse au traitement avec PEG-INF/RBV autres que le génotype du VHC incluent l'âge avancé, une fibrose avancée, un indice de masse corporelle élevé, une résistance à l'insuline et l'ethnicité africaine. Un polymorphisme spécifique hérité sur le chromosome 19 au niveau du SNP rs12979860, proche du gène de l'interleukine 28B (IL28B), est fortement associée à réponse virologique soutenue (RVS) dans tous les groupes de patients, indépendamment de tous les autres prédicteurs. Plusieurs autres études d'association indépendantes du génome ont également identifié des SNP supplémentaires, dans la région IL28B, associés à la réponse au traitement.
Chez les patients avec des prédicteurs de réponse favorable, l'observance du traitement est un facteur important de guérison. PEG-IFN et ribavirine sont tous les deux associés à des effets indésirables importants, tels que symptômes grippaux, fièvre, éruption cutanée, anorexie, troubles thyroïdiens, cytopénies (déficit quantitatif d'un certain type de cellule du sang (globules rouges ou blancs, plaquettes)) et troubles de l'humeur. Les effets secondaires entraînent une réduction de la dose chez 60-80% des patients et l'arrêt du traitement chez 5-10% d’entre eux.
De plus, de nombreux patients ne commencent jamais le traitement à cause de contre-indications médicales ou psychosociales (réelles ou perçues) soit l'IFN soit à la ribavirine. Beaucoup plus encore différent le traitement à cause d’histoires anecdotiques à propos des effets indésirables graves. Enfin, il y a un nombre important et croissant de patients GT1 principalement qui sont non-répondeurs au traitement PEG-INF/RBV, chez lesquels aucune alternative thérapeutique n'est disponible actuellement. De nouvelles approches thérapeutiques offrant des améliorations de l'efficacité, l’innocuité et la tolérance sont nécessaires d'urgence pour répondre à ces besoins médicaux non satisfaits.
On prévoit que l'association de plusieurs agents antiviraux à action directe (AAD) ciblant différentes étapes de la réplication du VHC devrait fournir un schéma posologique libre d’interféron. Les études, actuelles et à venir, permettront de déterminer quelle combinaison (des inhibiteurs de protéase, polymérase non nucléosidiques, polymérase nucléoside, NS5A et cyclophylline B), combien d'AAD et quelle durée de traitement seront nécessaires pour optimiser la guérison. Il sera également important de minimiser l'émergence de multi-résistances qui mettraient en péril les options de retraitement futur.
Les cinq étapes de la réplication du VHC qui sont des cibles potentielles pour des AADs incluent la liaison initiale du VHC aux hépatocytes récepteurs de surface (via LDLr (récepteur des lipoprotéines de faible densité) et CD81), la traduction et la transformation de la polyprotéine (via le complexe de la protéase du VHC), la réplication de l'ARN (via le complexe de la polymérase ARN-dépendante du VHC), l'assemblage et la maturation du virion, suivie par la libération de l'hépatocyte.
Un film d'animation du cycle de réplication du virus de l'hépatite C est disponible à l'Université Claude Bernard Lyon 1 ainsi qu'une page d'explication.
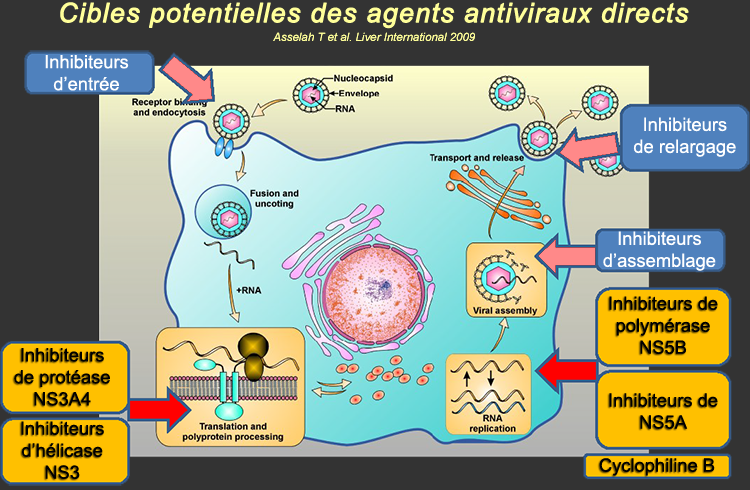
À ce jour, les approches les plus réussies sont le ciblage de la protéase (via l'inhibition de la protéase NS3A4) et de la polymérase du VHC (via l’inhibition de NS5A, NSAB et indirectement par NS3A4).
Les premiers AAD à être commercialisés sont les inhibiteurs de protéase, boceprevir et telaprevir, utilisés en addition au traitement PEG-INF/RBV. Les avantages en termes d'efficacité sont considérables : 48 semaines de boceprevir plus PEG-INF/RBV ont augmenté les taux de RVS chez les patients naïfs de traitement GT1 de 38 à 66%, tandis que 12 semaines de telaprevir suivies de 24 semaines PEG-INF/RBV ont augmenté le taux de RVS de 43 à 75%. La trithérapie offre aussi de l'espoir dans le traitement des patients déjà traités, en particulier les rechuteurs et les répondeurs partiels. Toutefois, tous les deux AAD ont des toxicités spécifiques (notamment anémie et dysgueusie avec boceprevir et anémie et éruptions cutanées avec telaprevir).
Bien que la trithérapie soit devenue le nouveau standard de soins à la fin de 2011, elle ne conviendra pas aux patients qui sont intolérants ou ont des contre-indications à la ribavirine ou à l’IFN, y compris les patients atteints de cirrhose décompensée ou après une transplantation d'organe. Telaprevir a une activité antivirale semblable contre le VHC GT2, mais n'a pas d'effet chez les patients atteints d’une infection au VHC GT3. Tous les inhibiteurs de protéase actuels et la plupart des inhibiteurs de polymérase non-nucléosidique en développement sont principalement actifs contre le VHC GT1. Le traitement PEG-INF/RBV restera le standard de soins pour les VHC non-GT1 jusqu'à ce que les inhibiteurs nucléosidiques de la polymérase et les inhibiteurs de cyclophylline entrent en pratique clinique.
Enfin, les 30 à 40% de patients GT1 qui ne répondent pas à cette nouvelle trithérapie auront développé une résistance aux inhibiteurs de protéase, ce qui limite les options de traitement futures.
Par conséquent, bien que l'ajout d'un seul DAA au PEG-INF/RBV peut améliorer la guérison et raccourcir la durée de traitement, cette approche ne pourra pas satisfaire les besoins du groupe des patients difficiles à traiter.
Le développement d'un traitement « tout oral », sans IFN, avec plusieurs AAD devrait résoudre ce besoin médical non satisfait et pourrait potentiellement devenir la norme de soins pour tous les patients présentant une infection chronique par le VHC.
Il y a une liste rapidement grandissante de candidats potentiels pour une telle association, y compris les inhibiteurs de l’hélicase NS3, les inhibiteurs de la protéase NS3/4A, les inhibiteurs de cyclophylline B, les inhibiteurs NS5A, les inhibiteurs NS5B nucléosidiques et non-nucléosidiques. Les essais cliniques de certains antiviraux à action directe sont décrits sur ce site.
Les principaux critères pour l'association des AAD sont :
- augmentation de l'efficacité antivirale sans augmentation de toxicité,
- absence de résistance croisée,
- prévention de l’échappement virologique du à l'émergence de mutants résistants à l'un ou aux deux AAD,
- absence d'interactions médicamenteuses et de toxicités directes croisées.
Le but ultime est de développer une combinaison de médicaments de prise orale sur une courte durée, sans IFN, avec une excellente innocuité, tolérance et efficacité chez tous les patients naïfs et préalablement traités.
Il y a actuellement plus de 50 nouvelles molécules qui sont testées dans différentes études cliniques. Les prochaines générations d'anti-protéases en développement de même que d'autres AAD (inhibiteurs de polymérases, de la cyclophilline et de NS5A) devraient être disponibles vers 2015. Les associations d'agents antiviraux directs sont en cours d'étude avec des résultats encourageants.





/http%3A%2F%2Fstorage.canalblog.com%2F38%2F75%2F857536%2F82798339_o.png)
/https%3A%2F%2Fassets.over-blog.com%2Ft%2Fcedistic%2Fcamera.png)
/https%3A%2F%2Fprofilepics.canalblog.com%2Fprofilepics%2F5%2F1%2F516944.jpg)